臨床の現場における薬剤師においても積極的に研究を行い、学会発表や論文投稿を行うことが求められておりますが、たとえアンケート調査を行い、その結果を発表する場合でも、インフォームド・コンセント、利益相反、個人情報の保護等、多岐にわたる配慮が必要となり、第三者による客観的な審査が必要となる場合があります。
人を対象とする医学系研究については、平成26年に「人を対象とする医学系研究に関する倫理指針」が制定・公布され、その後「人を対象とする生命科学・医学系研究に関する倫理指針」(令和3年文部科学省・厚生労働省・経済産業省告示第1号。以下「指針」)が制定され、令和3年6月30日より施行されました(令和4年3月一部改正)。
人を対象とした臨床・疫学研究の実施にあたっては、本指針に則って進めることが求められており、薬剤師が活動する分野の研究においても、倫理審査が必要かの判断、並びに必要なものについては倫理審査を受けることが必須となります。
●研究倫理指針について学びましょう
・人を対象とする生命科学・医学系研究に関する倫理指針(本文)(令和5年3月27日一部改正)
・人を対象とする生命科学・医学系研究に関する倫理指針ガイダンス(令和6年4月1日一部改訂)
・人を対象とする生命科学・医学系研究に関する倫理指針ガイダンス新旧対照表(令和6年4月1日)
・施行通知(令和5年3月27日)
・「人を対象とする生命科学系・医学系研究に関する倫理指針」説明資料(令和5年4月17日)
●研究倫理に関する研修を受講しましょう(必須)
「人を対象とする生命科学・医学系研究に関する倫理指針ガイダンス」では、「研究者等は、研究の実施に先立ち、研究に関する倫理並びに当該研究の実施に必要な知識及び技術に関する教育・研修を受けなければならない。また、研究期間中も適宜継続(少なくとも年に1回程度)して、教育・研修を受けなければならない」と定めています。
研究に関わる研究者等(研究責任者だけでなく、分担研究者も含む)は、研修倫理に関する研修を受け、申請時に研修終了証のコピーを添付しなければなりません。
※ 受講していない研究者は、受講するまで研究に関与できません。
◇神奈川県薬剤師会主催 研究倫理に関する研修会
(神奈川県薬剤師会主催研修会一覧よりご確認ください)
◇日本薬剤師会JPALS e-ラーニングコンテンツ
◇APRIN eラーニングプログラム(CITI Japan)
◇臨床試験のためのe-Training center
◇ICR臨床研究入門
●その研究は倫理審査が必要ではないですか
人を対象とする研究で学会発表、論文投稿の対象となるものについては、研究計画の立案時点で研究計画書を作成し、倫理審査を受けることが必要となる場合があります。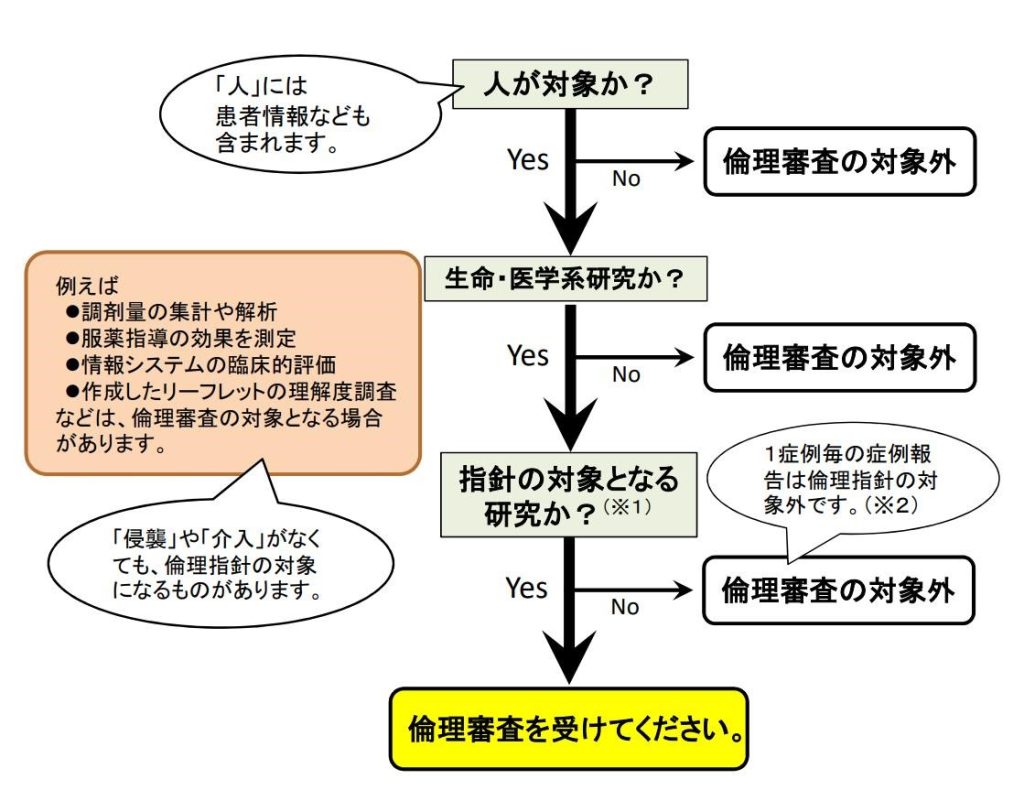
(※1)指針の対象となる研究はガイダンスに例が記載されていますので、ガイダンスp.4~p.6をご確認ください。
(※2)「症例報告」は、「研究に該当しない1症例毎の報告」の場合には該当しない、という解釈をしています。
複数症例についてデータをまとめて発表等を行う場合には、研究となり、倫理審査が必要となります。
なお、1症例報告で倫理指針上の臨床研究に該当せず倫理審査は不要とされても、個人情報保護法に則った対応が必要となる場合もあり、注意が必要です。
※詳細は「人を対象とする生命科学・医学系研究に関する倫理指針」及びガイダンスをご覧ください。
出典:日本薬剤師会 臨床・疫学研究推進委員会作成 「倫理審査対象研究フローチャート」Ver4(2022年7月)
★倫理審査が必要な研究テーマの例(2018年9月日本薬剤師会)
・ 患者に対してアドヒアランスをアンケート調査する研究
・ 吸入指導の前後に手技を評価する研究
・ 過去の薬歴を調査して、副作用発現率を明らかにする研究
★入門編 調査研究 アンケートをする前に
作成:東京都薬剤師会 発行:神奈川県薬剤師会 平成30年3月